标准电极电势标准氢电极原电池是由两个相对独立的电极所组成,每一个电极相当于一个“半电池”,分别进行氧化和还原反应
由不同的半电池可以组成各式各样的原电池
我们还未能在实验和理论上计算个别电极的电极电势,而只能够测得由两个电极所组成的电池的总电动势
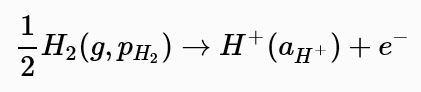
但在实际应用中只要知道与任意一个选定的作为标准的电极相比较时的相对电动势就够了
如果知道了两个半电池的这些数值,就可以求出由它们所组成的电池的电动势
按照1953年IUPAC(国际纯粹与应用化学联合会)的建议,采用标准氢电极作为标准电极,这个建议被广泛接受和承认,并于1958年作为IUPAC的正式规定

根据这个规定,电极的氢标电势就是所给电极与同温下的氢标准电极所组成的电池的电动势
氢电极的结构是:把镀铂黑的铂(把电镀法在铂片的表面上镀一层呈黑色的铂微粒铂黑)插入含有氢离子的溶液中,并不断用氢气冲打到铂片上
在氢电极上所进行的反应为在一定温度下,如果氢气在气相中的分压为p⊖(标准压强,即105Pa),且氢离子的活度等于1(即为1mol溶质/1L溶剂
一般溶剂都用水,在浓度较低时,活度近似等于浓度,所以也可以说是标准浓度,其值为1mol/L),即mH+=1mol·kg-1,γH+=1,am,H+=1,则这样的氢电极就作为标准氢电极
根据以上规定自然得出标准氢电极的电极电势等于零
实际测量时需用电势已知的参比电极替代标准氢电极,如甘汞电极、氯化银电极等
它们的电极势是通过与氢电极组成无液体接界的电池,通过精确测量用外推去求得的
以上内容由大学时代综合整理自互联网,实际情况请以官方资料为准。